Cell Culture FAQs: Bacterial Endotoxin Contamination
What is the difference between endotoxin vs. exotoxin?
Both are potentially hazardous to cell cultures. Exotoxins are toxic substances, usually proteins, secreted by bacteria and released outside the cell. Whereas endotoxins are bacterial toxins consisting of lipids that are located within a cell wall of the bacteria. Exotoxins are usually heat destroyed whereas endotoxins cannot be destroyed by high temperature. Exotoxins have high antigenicity and elicit an immune response whereas endotoxins do not.
How is endotoxin tested?
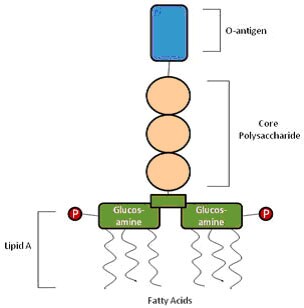
The limulus amebocyte lysate assay (LAL assay) is the most commonly used test for endotoxin. LAL (derived from the horseshoe crab) reacts with bacterial endotoxin lipopolysaccharide (LPS), which is a membrane component of gram-negative bacteria, to form a gel-clot which can be quantified. Endotoxin is measured in endotoxin units per milliliter (EU/mL). One EU equals approximately 0.1 to 0.2 ng endotoxin/mL of solution. Currently there are three forms of the LAL assay, each with different sensitivities. The LAL gel clot assay can detect down to 0.03 EU/mL while the LAL kinetic turbidimetric and chromogenic assays can detect down to 0.01 EU/mL.
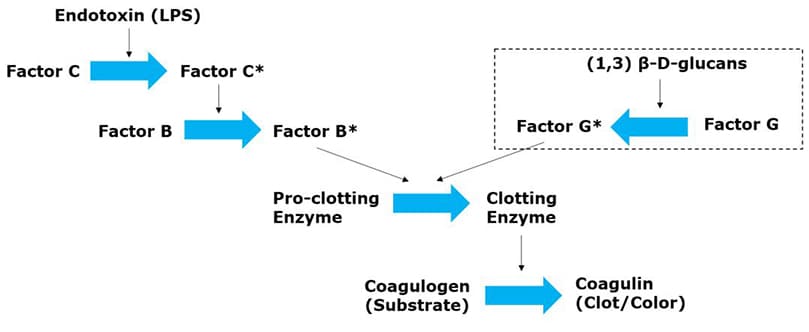
Figure 2.LAL assay test principle. The cascade of endotoxin detection in Limulus amoebocyte lysate (LAL) assay starts when the endotoxin LPS reacts with Factor C in and turn, activates the factor B. Factor B turns the gel-forming pro-enzyme into an enzyme. The resulting clotting enzyme is responsible for anchoring the two peptide units in the coagulogen, forming an insoluble gel. Other compounds which also cause the gelation in the amebocyte lysate of the horseshoe crab can interference in the test of bacterial endotoxins. Some of these compounds are (1,3)-β-D-glucans, which lead to false positives in the LAL test.
What are common sources of endotoxin contamination found in the lab?
Thorough cleanliness in all labware, media raw materials, and proper lab techniques are essential to substantially reduce endotoxin levels in the cell culture lab. It is also recommended to filter sterilize all media using a filtration device such as Stericup® filter unit which can eliminate all potential endotoxins before introducing to cells.
- Water: High purity water is essential to every laboratory. Milli-Q® Integral is a water purification system providing labs with ultrapure endotoxin-free water, directly from tap water. The system has the capacity to produce up to 300 L/day of pure and/or ultrapure water, satisfying the needs of most labs. In addition, we offer single use bottles of endotoxin free water for all cell culture applications.
- Serum: Due to its biological animal source, fetal bovine serum as historically been a major culprit for harboring endotoxin. However, improved screening has significantly reduced the risks. Every lot of our serum has been tested for endotoxin levels to ensure a high level of performance.
- Cell Culture Reagents: Common reagents like Ecoli. derived recombinant growth factors, hormones, lipids, basal media and dissociation reagents like trypsin can all be a source of endotoxin. We test all our cell culture tested reagent for endotoxin levels.
- Plasticware/Glassware: Glassware, plastic tubing and fittings should be pyrogen-free, and reusables should be rinsed with pyrogen-free or low-endotoxin water. Plastic bottles should be sterilized by gamma irradiation.
- User Contamination: Bacteria is present on all surfaces of skin, hair and saliva. Thus, proper aseptic technique while handling cell cultures is necessary to minimize the risk of introducing endotoxin into the system.
What are the effects of endotoxin on cell cultures?
Endotoxins affect both in vitro and in vivo cell growth and function and are a source of significant variability. In vitro, there is increasing evidence that endotoxin cause a variety of problems for cell culture research. Among the effects documented were the stimulation of leukocyte cultures to produce tissue factors, the induced production of IL-6 in equine macrophages, and the inhibition of murine erythroid colony formation by very low levels (less than 1 ng/mL) of endotoxin. In vivo, endotoxins elicit an inflammatory response in animal studies. The presence of endotoxin in products for injection (vaccines and injectable drugs) can result in pyrogenic responses ranging from fever and chills to irreversible and fatal septic shock.
What are the acceptable limits of endotoxin in cell cultures?
Due to the serious risks associated with endotoxin contamination, the US Food and Drug Administration (FDA) has set limits on concentration of endotoxin for medical devices and parenteral drugs that researchers should be aware of. Current FDA limits require eluates from medical devices to be less than 0.5 EU/mL unless the device comes into contact with cerebrospinal fluid where the limit is then 0.06 EU/mL.
How do you prevent endotoxin contamination?
It is essential to use endotoxin tested reagents, supplements and media from a trusted reagents supplier. It is also important to user proper aseptic techniques and thoroughly rinse and sterilize all cell culture plasticware and consumables like pipettes and conical tubes before culturing cells.
How to remove endotoxin if cultures become contaminated?
It is recommended to discard all reagents and cells if cultures become contaminated with endotoxin and start with new reagents and cells. However, if sample cannot be discarded reagents can be used to eliminate them. These endotoxin removal solutions rely on the micellar properties of Triton X-114 to remove LPS endotoxins from samples.
Materials
如要继续阅读,请登录或创建帐户。
暂无帐户?