样品纯化
精选分类
以下是一些最常用的纯化技术,实验室中常用于制备样本以供后续分析。
透析
透析是一种用于从样品中去除盐分或其他低分子量分子的纯化技术。它还用于改变样品的缓冲液组成。透析是一种被动技术,需要大量缓冲液。
缓冲液置换与脱盐
脱盐是一种从样品中去除盐类及其他低分子量污染物的简便方法。该方法还用于不同色谱步骤前后的缓冲液置换,以及快速去除试剂以终止反应。
分级沉淀
分级沉淀用于从少量样品中去除粗杂质。沉淀技术基于溶解度差异原理对组分进行分离。由于不同蛋白质在疏水性程度上存在差异,提高盐浓度可增强蛋白质之间的疏水相互作用,从而引发沉淀。
萃取
通过萃取进行样品制备,旨在从复杂样品或体积庞大的样品中分离出目标分析物。 该过程可去除可能堵塞HPLC和GC色谱柱的干扰组分,并将分析物浓度提高100至5,000倍,从而显著提高检测灵敏度。作为选择性与特异性样品制备的重要环节,萃取有助于确保色谱分析结果的可靠性。萃取方法包括液-液萃取、固相萃取(SPE)和固相微萃取(SPME)。
亲和色谱
亲和色谱基于蛋白质与已偶联至色谱基质上的特定配体之间的可逆相互作用来分离蛋白质。该技术具有高度选择性,可实现高容量的蛋白质纯化。只要针对目标蛋白有合适的配体可用,即可采用亲和色谱法。
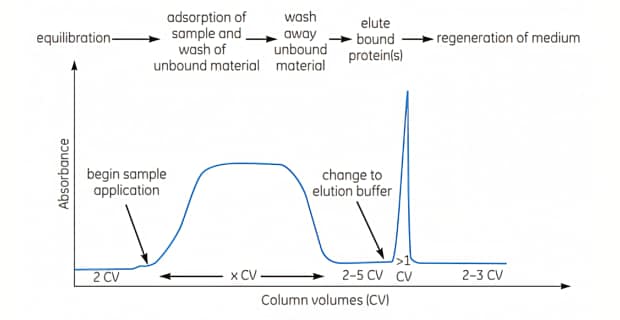
亲和色谱纯化包括捕获和洗脱两个步骤。在捕获阶段,目标蛋白与固定在色谱基质上的互补配体发生特异性且可逆的结合。其目的是分离、浓缩并稳定目标产物,同时保持其效价和活性。 在洗涤色谱柱以去除未结合物质后,通过改变条件至有利于洗脱的状态,即可回收结合的目标蛋白。洗脱可通过使用竞争性配体进行特异性洗脱,或通过改变pH值、离子强度或极性进行非特异性洗脱。洗脱使目标蛋白能够以纯化且浓缩的形式被收集。
相关文章
- 如果物质相互溶解形成均匀的溶液,就可以说它们相互混溶。收藏或下载我们的常见实验室溶剂混溶性表。
- How to separate proteins and peptides with affinity for metal ions by immobilized metal chelate affinity chromatography.
- This page shows volatile and non-volatile buffer suggestions for anion and cation exchange chromatography.
- Ion exchange chromatography is employed by the Genopure Plasmid Midi Kit and the Genopure Plasmid Maxi Kit.
- 实验室规模的脱盐是一种成熟、简单、快速的方法,可以在将样品转移至所需缓冲液的同时快速去除低分子量污染物。
- 查看全部 (31)
相关协议
- 默克干货知识分享,在比较不同尺寸色谱柱的结果时,使用线性流速(cm/小时)来表示流量会更方便。但是,流量通常采用体积流量(mL/min)的形式测定。通过使用以下公式可实现线性流速与体积流速之间的相互换算。
- Separation using Sephadex LH-20 column for Size Exclusion Chromatography media in polysaccharide network from Cytiva.
- In this section the practical aspect of Reverse Phased Chromatography ( RPC) is discussed including media and column selection and eluent selection and preparation.
- Superose from Cytiva are Size Exclusion Chromatography media consisting of a composite base matrix of dextran and agarose. This page shows how to perform a separation with a superose column.
- The Amberlite™ XAD-4 resin used in Porozorb™ cartridges is a proven technology that is highly effective in removing various detergents from cell culture media for biopharmaceutical applications such as vaccine production.
- 查看全部 (49)
查看更多文章和操作规程
我们能为您提供什么帮助
如有任何疑问,请提交客户支持请求;
或联系我们的客服团队:
发送邮件至
custserv@sial.com 或致电 +1 (800) 244-1173
其他支持
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- 计算器与应用_缓冲液计算器_HPLC方法转换计算器-默克生命科学
默克该工具箱包括用于化学、生命科学、材料科学等方面的科学研究工具和资源。
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.