如何使用mPAGE® Lux凝胶浇铸系统更快地浇铸SDS-PAGE凝胶
探索mPAGE® Lux铸胶系统,3分钟即可获得即用型SDS-PAGE凝胶。新鲜SDS-PAGE凝胶,随时待命。感兴趣?立即下方索取信息。
凝胶浇铸轻松搞定
如何制作SDS-PAGE凝胶?传统凝胶浇铸需分步操作分离胶与堆叠胶,过程耗时费力。研究人员在满足凝胶浇铸与电泳需求时,可选方案向来有限。 我们创新的mPAGE® Lux SDS-PAGE凝胶浇铸系统,兼具手工浇铸凝胶的灵活性与预制凝胶的可靠性,既不牺牲质量,也无需耗费时间,更避免了替代方案带来的高昂成本。使用mPAGE® Lux浇铸系统,三分钟内即可完成凝胶制备。告别传统凝胶制备方法中耗时费力的手工步骤,体验全新效率。

采用精密系统控制的一步光聚合技术,配合简化的制备步骤,有效降低操作失误风险。我们的mPAGE®铸胶系统可防止渗漏,而双-Tris凝胶相较于手工浇铸的Tris-甘氨酸凝胶,能提供更优异的条带质量。 此外,mPAGE® Lux试剂盒、mPAGE® TurboMix试剂盒及mPAGE®预制凝胶均采用双-Tris化学体系,并兼容相同的电泳缓冲液与凝胶染色剂。mPAGE® Lux浇铸系统无需使用APS或TEMED,通过减少有毒化学品用量提供更安全的操作方案。
为进一步提升兼容性并满足您的工作流程需求,我们现推出mPAGE®夹扣式掩模。使用mPAGE®夹扣式掩模时,Bio-Rad Mini-PROTEAN®短板、间隔板和梳板,以及mPAGE®迷你短板、间隔板和梳板均可配合固化系统——mPAGE® Lux固化工作站——进行凝胶固化。
注:使用夹扣式遮罩时,mPAGE® Lux遮罩短板不再需要,但遮罩短板仍可继续使用。
传统手工浇铸工作流程
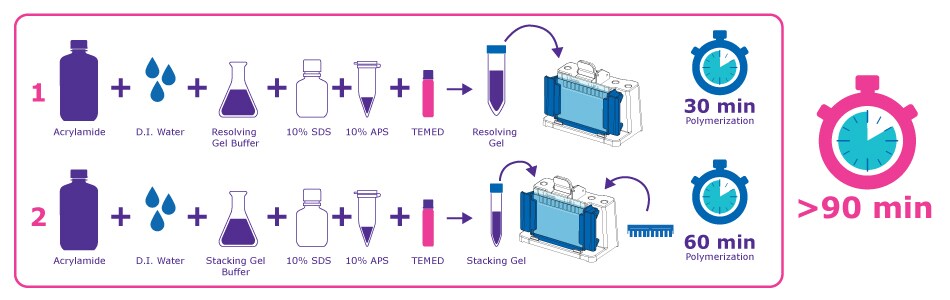
图1.传统手工浇铸SDS-PAGE凝胶工作流程信息图,展示了扩展步骤及90分钟或更长的聚合时间。
mPAGE®Lux 工作流程
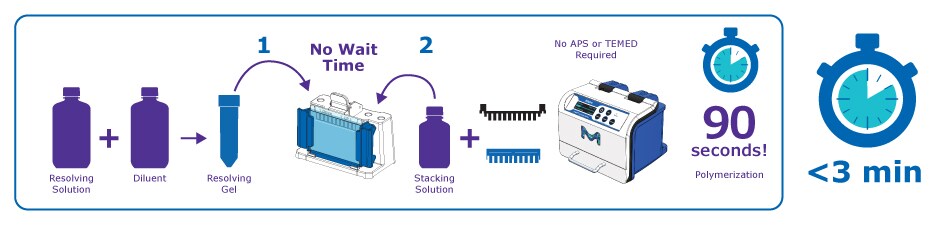
图2.传统凝胶浇铸与mPAGE® Lux工作流程对比。相较于传统凝胶浇铸技术,mPAGE® Lux浇铸系统整体步骤更少、聚合时间缩短且有毒废弃物更少。通过mPAGE® Lux浇铸系统制备的凝胶可兼容mPAGE® Mini凝胶槽及Bio-Rad Mini-PROTEAN®细胞。 为获得卓越分辨率并缩短运行时间,请选用我们的mPAGE®缓冲液。mPAGE® Lux凝胶兼容双-Tris兼容缓冲液及染色试剂。
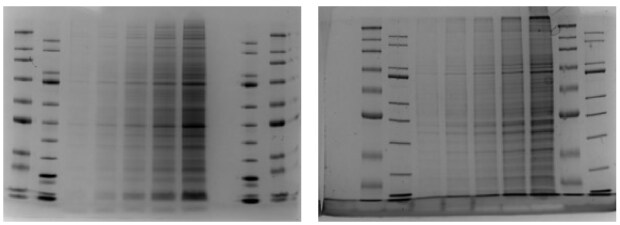
图3.mPAGE® Lux Bis-Tris凝胶与手工浇铸甘氨酸-Tris凝胶的数据质量对比。左侧为mPAGE® Lux Bis-Tris凝胶的条带质量,右侧为手工浇铸甘氨酸-Tris凝胶。两种凝胶均为10%丙烯酰胺,均加载A431人细胞裂解物梯度样品。 电泳运行时间:Lux凝胶为200V下42分钟,甘氨酸三羟甲基氨基甲烷凝胶为120V下119分钟。凝胶采用ReadyBlue™考马斯亮蓝染色剂进行染色。
mPAGE® Lux凝胶浇铸系统为您的凝胶浇铸流程提供创新解决方案。您无需再在节省时间与节约资源之间做出取舍。这款新型凝胶浇铸系统让研究人员能够在需要时快速轻松地浇铸凝胶,其成本仅为预制凝胶技术的零头。采用mPAGE® Lux凝胶浇铸系统,提升实验室效率,升级凝胶电泳工作流程。
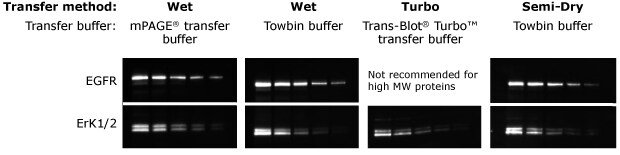
图4.Western blotting技术中湿法、快速法与半干法转印方法的比较。实验采用12% mPAGE® Lux Bis-Tris凝胶,通过梯度浓度的A431人细胞裂解液进行电泳,并采用不同转印方法将蛋白质转移至Immobilon®-P膜上。 膜先经抗EGFR和抗ErK1/2抗体孵育,再使用Immobilon® ECL Ultra Western HRP底物进行显色检测。Turbo法=采用Bio-Rad Trans-Blot® Turbo™转移系统及Trans-Blot® Turbo™转移试剂包进行转移。


图5. mPAGE® Lux Bis-Tris凝胶的重复性。A. 制备四块8%凝胶,分别进行A341人细胞裂解液梯度电泳,随后使用ReadyBlue™考马斯亮蓝染色。B. 计算每块凝胶中未染色分子量标记物的相对迁移距离(Rf)。每条蛋白带均显示标准偏差。
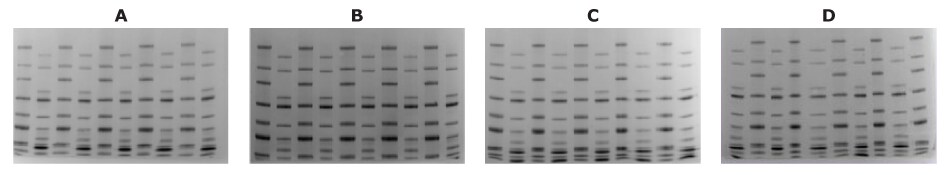
图6.mPAGE® Lux Bis-Tris试剂保质期分析。使用(A)0个月、(B)6个月、(C)12个月或(D)24个月的试剂制备的mPAGE® Lux Bis-Tris凝胶。未观察到电泳图谱或运行时间存在差异。

图7.mPAGE® Lux固化工作站。
mPAGE® Lux Bis-Tris试剂盒是专为mPAGE® Lux铸胶系统设计的专用试剂套件。该试剂盒包含3个组分:分离溶液、稀释液和堆叠溶液。 该试剂盒适用于8.0%-13.5%浓度的多种丙烯酰胺凝胶。mPAGE® Lux试剂盒的描述及配置如下:
mPAGE® Lux SDS-PAGE凝胶浇铸方案
所有溶液必须避光保存以防止聚合。浇铸凝胶前,将所有溶液恢复至室温。
分离凝胶
- 将分离溶液与稀释液混合制备分离凝胶溶液。具体配比体积参见下表。可预先批量配制分离凝胶溶液以连续制作多个凝胶。
- 使用洁净移液器将分离溶液加入黑色混合管或其他不透明容器中。
- 使用清洁移液器向同一混合管中加入稀释剂。
- 通过轻柔翻转容器进行混合,切勿使用涡旋混合器。
分离凝胶溶液配制体积
制作单层1.0mm凝胶时使用以下体积。0.75mm及1.5mm凝胶的溶液体积请参阅产品页面完整用户指南。
上层电泳凝胶
上层溶液可直接从瓶中取用。每1.0毫米凝胶需使用1.5毫升上层溶液。重要提示:请勿稀释上层溶液。
凝胶浇铸
- 用中性洗涤剂清洁玻璃板,用去离子水冲洗。使用前用70%乙醇擦拭。
- 使用mPAGE®间隔板与mPAGE® Lux遮罩短板组装mPAGE®凝胶浇铸器,形成玻璃卡匣。遮罩短板应使文字朝向卡匣左侧。关闭浇铸器夹具前,确保两块玻璃板在浇铸器框架底部对齐。注意:mPAGE® Lux遮罩短板必须配合mPAGE®固化站使用。
- 按下电源按钮启动mPAGE® Lux固化站。设备将自动执行自检程序,完成后显示就绪界面。
- 开启门板,将凝胶铸模架置入固化站,确保铸模架后端与缓冲挡块对齐。
- 使用洁净的5毫升移液器,将配好的分离凝胶溶液注入mPAGE®凝胶浇铸器框架标示的注液线位置。
- 使用洁净的5毫升移液器,缓慢注入堆叠溶液至短板顶部。
- 将mPAGE®梳板以倾斜角度缓慢插入,避免梳齿间形成气泡。重要提示:混合使用不同孔板规格可能导致孔板成型异常。使用规格:
- 10孔梳配合10孔mPAGE® Lux遮蔽短板
- 15孔梳配合15孔mPAGE® Lux遮蔽短板
- 擦拭短板前沿溢出的溶液,防止溢出区域固化不完全。
- 将卡扣式掩膜安装于短板及浇铸框架上方。
- 遮罩前缘应紧密贴合短板,完全覆盖梳齿。
- 关闭固化站门并选择凝胶厚度。
- 按下开始键启动凝胶固化。提示:若需浇铸多块凝胶,可在第一块凝胶固化时,立即启动第二台凝胶浇铸仪进行浇铸。
- 固化完成后,打开门取出凝胶浇铸器。通过松开张力夹释放浇铸框架,将盒体从凝胶浇铸器中取出。随后打开框架两侧,从顶部滑出盒体。
- 凝胶需立即使用,或用湿纸巾包裹卡匣,平放于密封袋或其他密闭容器中,于2-8°C环境下保存最长2周。切勿暴露卡匣,否则凝胶将干燥失效。

图8.使用MOPS SDS电泳缓冲液和MES SDS电泳缓冲液的mpage® Lux Bis-Tris凝胶迁移图谱(kDa)。
电泳后如何去除凝胶
使用凝胶刮刀从玻璃卡匣中取出凝胶。沿凝胶边缘(右侧)切割以避免凝胶撕裂。mPAGE® Lux Bis-Tris凝胶仅适用于MOPS-SDS或MES-SDS电泳缓冲液。Bis-Tris凝胶与Tris-Glycine电泳缓冲液不兼容。
采用mPAGE® Lux凝胶浇铸系统实现可持续凝胶浇铸
为量化mPAGE® Lux浇铸系统的可持续性影响,我们将其与代表性快速浇铸试剂盒(用于手工浇铸蛋白质电泳用聚丙烯酰胺凝胶)进行了对比计算。两种系统均需使用可重复使用的浇铸试剂盒及手工浇铸试剂盒。 mPAGE® Lux浇铸系统额外需要使用mPAGE® Lux凝胶固化站,而基准系统则需使用APS和TEMED(这两种试剂需与手工浇铸试剂盒分开购买)。
本评估涵盖mPAGE® Lux固化站5年最低使用寿命周期内电泳凝胶浇铸所需全部组件,包括手工浇铸试剂盒、必需试剂及所有耗材的实验室器具在内的生产、包装、分销、使用及报废处理全过程影响。 计算基于每年生产250、500或1000块凝胶的场景,并宣称其与基准系统的最低差异。
材料与产品可持续性属性
mPAGE® Lux浇铸系统虽为手工浇铸聚丙烯酰胺凝胶提供创新工作流程解决方案,仍需使用部分塑料耗材及危险试剂。尽管该应用中尚无丙烯酰胺的合适替代品,但系统已消除所有其余化学危害,且所需塑料耗材量较基准系统显著降低。
如图表所示,mPAGE® Lux铸胶系统所需的凝胶固化站额外质量,被凝胶铸造工作流程中所需产品的减少所抵消。在仪器整个生命周期内,系统总质量较快速铸胶系统至少降低20%。
每年浇铸500块凝胶时的系统总质量(kg):
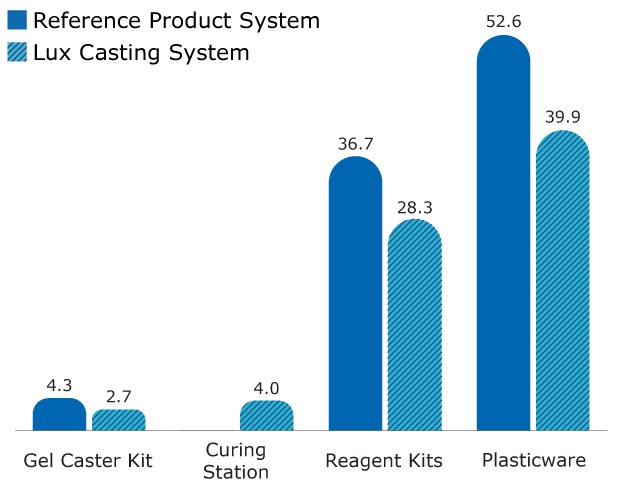
图9.mPAGE® Lux 凝胶电泳系统与对照产品系统年产500块凝胶的系统总质量(千克)对比。深蓝色=对照产品系统。浅蓝色=mPAGE® Lux 凝胶电泳系统。
此外,本产品遵循SMASH包装原则——这是我们通过减少包装用量、采用更可持续的材料以及简化回收流程来推动包装可持续性改进的战略。
- 产品及功能单元所需附加物品的包装量较基准系统减少30%。
- 系统内所有纤维类包装材料均获得可持续林业认证。
- 所有防护泡沫内衬均采用100%再生聚乙烯制成。
- 包装中不含有任何可能阻碍回收的材料,符合SMASH指南规定。
mPAGE® Lux铸造系统分销与产品使用
通过减少必需耗材及淘汰特定试剂,显著降低运输相关影响。在仪器最低使用寿命周期内,常规运输组件及配套包装的总减重至少达24%。
虽然新增仪器在运行时需要消耗能量,但mPAGE® Lux凝胶铸造工作站的设计充分考虑了节能需求。通过采用LED照明和简洁直观的用户界面,整体能耗水平始终保持在极低水平。 固化1000块凝胶的累计能耗仅为1.65千瓦时,相当于约33小时的笔记本电脑使用量。凝胶浇铸全流程中产生的一次性塑料废弃物至少减少25%。此外,mPAGE® Lux试剂在环境光照下可自聚合,彻底消除废弃物流中未聚合的丙烯酰胺残留。
通过按需浇铸新鲜即用凝胶,彻底规避了预制凝胶闲置的风险。mPAGE® Lux系统无需囤积试剂盒或预制不同浓度的凝胶,从而减少因组分过期产生的废弃物。mPAGE® Lux固化站属于电子设备,处置时须严格遵守所有适用法规。 有关电子废弃物处置的更多信息,请访问我们的《WEEE合规页面》。
本产品在整个生命周期中较基准系统展现出显著改进,已被认定为更环保的替代产品。更多详情请参阅我们的可持续设计框架及更环保替代产品页面。
采用mPAGE® Lux系统实现凝胶内蛋白质检测的快速可视化(无需染色)
SDS-PAGE是通过分子量分离蛋白质及其他生物分子的常用技术。凝胶内蛋白质可采用成熟的比色或荧光染色法检测,如考马斯亮蓝(CBB)、银染法及SYPRO™ Ruby染色。这些染色方法灵敏度各异,且常需耗时较长的孵育步骤。
三氯乙醇(TCE)最初被描述为荧光淬灭剂,该化合物通过紫外光激活产生新荧光团,可将色氨酸荧光从天然发射波长(~350 nm)向可见光(~512 nm)偏移。1-3 Kazmin等研究者利用TCE及其他三氯化合物的这一特性,开发出快速灵敏的一步法凝胶染色方案。4 随后研究将TCE直接掺入SDS-PAGE凝胶制备过程,实现了无需繁琐染色步骤的蛋白质检测。5,6 本文将介绍采用含TCE的mPAGE® Lux凝胶制备方法,实现无需染色的凝胶内蛋白质检测。
染色法与免染色法对比
通过对比TCE可视化与考马斯亮蓝染色法,发现两种方法的检测灵敏度相当(图10)。但基于TCE的检测无需染色步骤,可节省至少两至数小时的制备时间(具体取决于当前染色方法)。
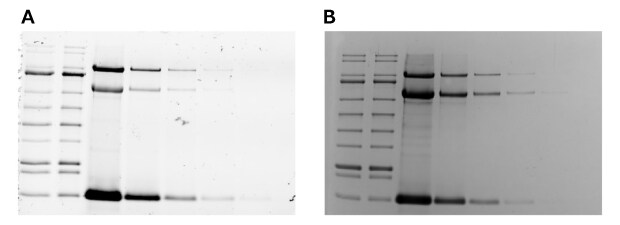
图10.TCE染色法与READYBLUE®考马斯亮蓝凝胶染色法在蛋白质可视化方面的比较。三种纯化蛋白(溶菌酶(14.4 kDa)、牛血清白蛋白(66 kDa)、 磷酸化酶b(97 kDa))分别以4 µg、1 µg、0.25 µg、0.0625 µg、0.0156 µg、0.004 µg、0.0009 µg及0 µg的浓度加载于含1% TCE的12% mPAGE® Lux凝胶中。 在MOPS-SDS电泳缓冲液中以200伏电压运行凝胶42分钟。(A)经TCE活化45秒后的蛋白质显影结果。(B)对应的READYBLUE®考马斯亮蓝染色凝胶图像。TCE诱导凝胶与考马斯亮蓝染色凝胶显示出相似的蛋白质检测灵敏度。
方法兼容性
本方法与下游分析(本例为蛋白质印迹)的兼容性亦进行了验证。图11展示了含TCE与不含TCE制备的蛋白质印迹对比。如图所示,当蛋白质印迹凝胶经45秒活化处理并在转印前成像时,可获得相似的免疫检测灵敏度。
然而,由于mPAGE® Lux凝胶聚合的特性,更长的活化与曝光时间可能影响蛋白质转移效率。蛋白质转移过程可能需要优化。若TCE显色后需进行Western blotting,建议采用最短活化时间,因为活化过程会影响mPAGE® Lux凝胶的转移效率。
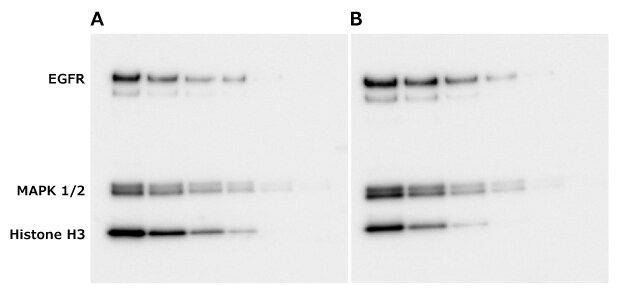
图11.TCE显影后的Western Blot实验。将EGF刺激的A431细胞裂解液(10 ng – 0.3 ng)制备成2倍稀释系列,分别加载至含(B)或不含(A)1% TCE的8% mPAGE® Lux凝胶中。 凝胶在MOPS-SDS电泳缓冲液中以200伏电压运行38分钟,含TCE的凝胶随后激活45秒并成像。两组凝胶均转移至Immobilon® P PVDF膜,采用标准免疫检测方法对膜进行EGFR、MAPK 1/2及组蛋白H3的探测。
无染色技术结合TCE活化
由于该TCE活化法无需额外染色步骤,可节省时间并在电泳后立即操作。结果表明,其蛋白质检测灵敏度与其他采用染色的传统方法相当。
总体而言,使用mPAGE® Lux凝胶及其他mPAGE®电泳产品,可快速且可重复地制备和运行凝胶。 此外,mPAGE® Lux凝胶与本文所述的TCE无染色技术兼容,可进一步简化现有实验流程。这为科研人员提供了宝贵工具——既能延续mPAGE® Lux浇铸技术的便捷性与灵活性,又可获得快速蛋白质可视化的附加优势。
mPAGE® Lux 铸造系统
mPAGE® Lux 配件与试剂
参考文献
如要继续阅读,请登录或创建帐户。
暂无帐户?