LC/MS/MS法测定谷物中的草甘膦、AMPA和草铵膦
简介
草甘膦是世界上最常用的除草剂之一。在玉米、大豆、棉花等转基因抗草甘膦作物问世后,其使用量显著增加。目前,每年有超过 14 亿磅的草甘膦用于田间。1美国环保局法规文件美国联邦法规 (CFR) 第 40 篇第 24 卷规定了食品和农产品中允许的草甘膦浓度。2
EPA 允许的谷物草甘膦残留(也称为作物组 15)浓度设定为 30ppm。其中不包括大米、大豆和玉米。大米中的允许浓度是 0.1 ppm,而在甜玉米中是 3.5 ppm。2对于草铵膦 (glufosinate)——一种在分析方法中经常与草甘膦一起使用的除草剂,谷物中的容许浓度为 0.4 ppm,大米中的容许浓度为 1.0 ppm。这些允许浓度包括代谢物和降解物。因此,草甘膦代谢产物(氨甲基)-膦酸 (AMPA) 也包括在本研究中(图 1)。
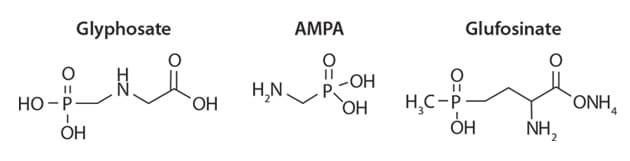
图 1.草甘膦、AMPA和草铵膦的结构
由于草甘膦广泛用于大豆和玉米的生产,因此在这些商品中可能会找到。在本应用中,我们重点探索了其他用于制作早餐(包括婴儿谷物制品)的谷物(燕麦和小麦)中是否存在草甘膦。
在过去的 30 年里,草甘膦分析方法不断进步。用邻苯二甲醛进行荧光检测时,需要对 HPLC 分析物进行衍生化。3一种利用芴甲氧羰基氯 (FMOC) 和荧光检测进行草甘膦衍生化的方法已被一些实验室提出和使用。4最近,随着现代更灵敏、更坚固的 LC/MS/MS 仪器的出现,无需衍生化即可分析草甘膦及其代谢产物已成为可能。本文采用 MS/MS 直接分析草甘膦。
实验
为了确认方法的效果,使用了有机速溶燕麦片和有机全麦面粉。扫描这些食物后没有发现存在草甘膦。全麦面粉按原样使用,速溶燕麦在使用前研磨。对于方法效果研究,两种基质均加标至含 100ppb 草甘膦和 100ppb 草铵膦。
燕麦也被加标到含有 100ppb 的 AMPA。我们还购买了有机玉米粉并测定其中的草甘膦,结果并未检出。同样的方法也可用于检测玉米粉和玉米制品。
对于筛选研究,使用开发的方法测定了以下基质之中的草甘膦含量:白面粉、即食燕麦片、婴儿米饭谷物、婴儿燕麦谷物和婴儿混合谷物。
样品预处理
该提取方法基于欧盟 (EU) 制定的水果和蔬菜的 QuPPe (极性杀虫剂快速分析法)方法,使用含有甲酸的水:甲醇 (50:50) 作为最终提取溶剂。5将 5 克均质谷物或谷物样品称入 50 mL 离心管中。加入水 (10 mL) 和 100 μL 内标溶液(水中的20 μg/mL 每种分析物)。然后将样品静置 30 min 至 2 小时。之后,加入 10 mL 含有 1% (v/v)甲酸的甲醇。样品在实验室振荡器上混合 15 min 并离心。在验证过程中使用了两种样品(燕麦和小麦),得到了的提取物明显不同。燕麦产生的提取物呈透明黄色,小麦提取物混浊且难以过滤。结果,我们对不同的谷物样品采用了两种不同的样品纯化程序。
SPE纯化样品
对于提取和离心后没有颗粒的样品,应用 Supel™-Select HLB 柱进行固相萃取 (SPE) 净化,类似于 Chamkasem 和 Harmon 报道的方法。6依次使用100% 甲醇以及含有0.5%(v/v)甲酸的水:甲醇(50:50)对 HLB 柱进行调理。对于 1 mL SPE 柱,使用 0.5 mL 样品提取物进一步调节小柱。丢弃来自该调节步骤的洗脱液。将第二份样品提取物 (0.5 mL) 装入 HLB 小柱中。收集洗脱液并通过 0.2 微米聚丙烯滤膜小瓶过滤。
使用超滤进法行样品净化
超滤装置用于清理在离心步骤后有微粒样品提取物,如小麦。在本次作业中使用截留分子量为 3 kDa 的聚醚砜膜 (MWCO)。为了使草甘膦的保留时间保持一致,将 0.5 mL 提取溶剂通过 4000 rpm 离心 5 min 对膜进行预处理。弃去该传递溶剂并装载 1 mL 样品提取物。通过 4000 rpm 离心 45 min 进行超滤。我们还确定了,含有再生纤维素膜的超滤装置(如带有 3 kDa MWCO 的 Amicon™Ultra 离心过滤器)无需预处理即可用于此步骤。收集并分析通过膜的透明样品。为了分析,使用低吸收小瓶来防止玻璃表面上分析物的损失。
啤酒样品制备
可以使用相同的方法分析啤酒样品。首先,将啤酒样品放入超声波浴中 15 min,彻底脱气。然后将 5 mL 啤酒样品与 5 mL 含 1% 甲酸的甲醇和内标混合。使用 SPE 程序将该样品短暂混合并清洁。
LC/MS/MS 方法
用于此分析的 HPLC 色谱柱是基于聚合物的apHera™ NH2色谱柱,可在pH 2 至 13条件下稳定、可靠地液相分离。流动相梯度在 pH 9 时使用水和碳酸铵。该流动相保证了结构中含有磷酸基团的草甘膦的正确电离,并在负 ESI 条件下进行检测。此外,碳酸铵缓冲液易挥发,且与 LC/MS 仪器完全兼容。 表 1 列出了所有分析物的 MS 条件, 图 2 列出了标准注射液的色谱图。使用 AB Sciex QTrap 3200 仪器进行分析。这种方法灵敏度有限。然而,如下所示,在本研究中,该方法能够量化大多数样品中的草甘膦污染。
结果
方法性能
SPE 和超滤净化方法都提供了良好的样品纯化效果,并且可用于 LC/MS 分析。在燕麦片中,所有三种分析物均在 100ppb 下检测和定量。在小麦粉中,草甘膦和草铵膦定量为 100ppb。方法测试的结果请见表 2。小麦样品方法产生的不确定度稍高,RSD 高达 19%。小麦方法没有使用 SPE 清理,与使用 SPE 清理的样品(如燕麦)相比,发现产生的信号具有更高的离子抑制。一般而言,所有样品中都存在不同程度的离子抑制,从 50% 到 80%,因此使用内标进行准确定量非常重要。
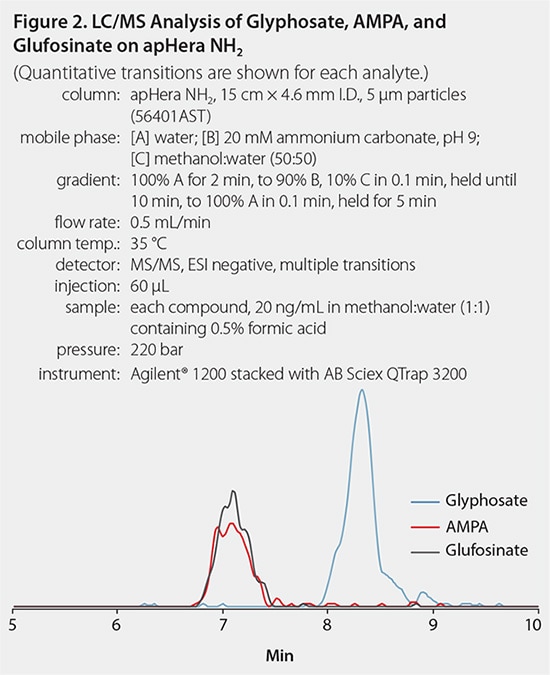
图 2.在apHera NH2色谱柱上LC/MC分析草甘膦、AMPA和草铵膦
啤酒中的草甘膦
在测试的啤酒中没有发现分析物。因此,啤酒样品中加入 50ppb 的草甘膦和草铵膦并进行分析。结果显示在表 2中。在这项工作中,我们没有尝试进一步筛选啤酒。
谷物中草甘膦的鉴定与定量
谷物中草甘膦的定量结果见表 3。即食燕麦片(图 3)和白面粉样品分别含有大量的草甘膦,1.2 和 0.8 ppm。有机燕麦片样品不含有可检测量的草甘膦(图 4)。婴儿谷物的草甘膦含量非常低。由于基体和结果的相对标准偏差较高,其含量接近仪器灵敏度的极限。婴儿燕麦谷物含有 1.1ppm 的草甘膦,婴儿混合谷物含有 0.25ppm 的草甘膦。没有一种婴儿谷物被贴上有机标签。在任何谷物产品中均未发现草铵膦。仅在速溶燕麦片中发现低水平的 AMPA。
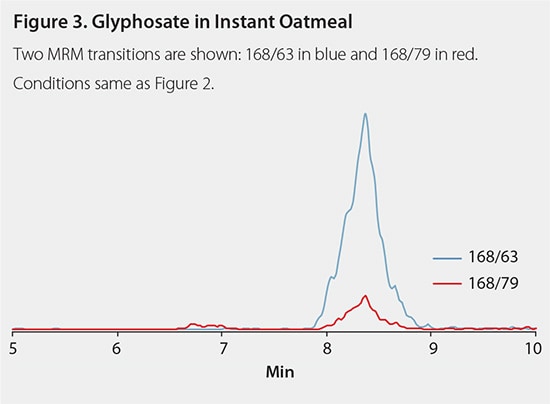
图 3.即食燕麦片中的草甘膦
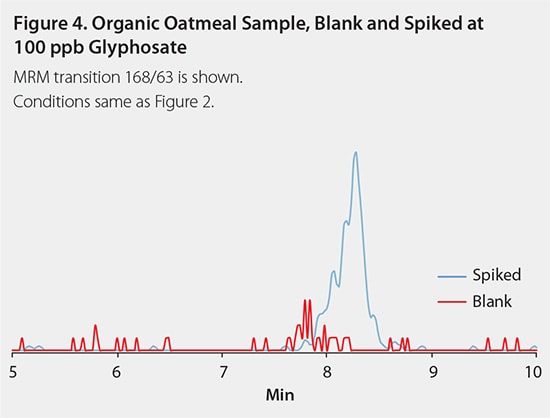
图 4.空白和掺入100ppb草甘膦的有机燕麦样品
结论
为草甘膦和相关化合物开发的建议方法使用 LC/MS/MS 检测和基于离子交换聚合物的 apHera NH2 色谱柱(在较高 pH 条件下稳定)。为此开发了从谷类食品中提取草甘膦的样品制备方法。该方法包括使用聚合物 SPE (该方法已成功地应用于谷物样品,包括燕麦片和婴儿谷物产品)进行纯化。包括超滤在内的清理工作是为含小麦的产品开发的,并成功应用于小麦粉样品。使用同位素标记的标准品可提高草甘膦测定的准确度,并可通过补偿样品中存在的电离效应而使用基于溶剂的校准曲线。事实证明,该方法可靠、表现良好,即使使用较旧和较不敏感的仪器。
材料
参考文献
如要继续阅读,请登录或创建帐户。
暂无帐户?