蛋白质SEC的色谱柱和分析标准品
蛋白质大小排阻色谱法测定分子量

体积排阻色谱法(SEC)已很好地用于蛋白质表征。从重组蛋白用于制药的早期发展开始,该技术就被用于生物制品的质量控制,并且该方法也不断地改进。如今,业内针对特定分离任务和即用标准开发了 (U) HPLC色谱柱,有助于促进方法开发并提高SEC方法的稳健性。
每当样品包含需要根据大小进行分离和表征的分子时,都可以使用分析尺寸排阻色谱法。该技术使用高度多孔的颗粒填充至色谱柱中。根据样品中分子的大小不同,有些分子可能会进入所有的孔隙,有些能够进入部分孔隙或无法进入任何孔隙。基于这种分配原理,最大的分子首先被洗脱,然后是尺寸逐渐变小的样品组分。一旦样品成功分离,样品的分子大小可以使用两种基本检测方法进行确定。静态光散射为分子质量测定提供了机会。分子量由光散射信号和折射率信号进行计算,并且不受分子的水合壳厚度影响。这种方法的缺点是设备成本较高,同时光散射检测器容易受到背景噪声的干扰。尽管光散射在许多应用中运用成熟,但是有时更经典的分子尺寸测定方法优于静态光散射。
尺寸排阻色谱校正曲线
为了生成蛋白质SEC校正曲线,将由各种已知大小的分子组成的校准混合物注入与样品所用的同一色谱柱中。从校准色谱图中获得每种组分的保留时间,并针对对数分子量作图。为开发用于分析免疫球蛋白G的三个U(HPLC)色谱柱,绘制了校准曲线(图1)。TSKgel® SuperSW mAb HTP用于快速简便地从HPLC转换至快速UHPLC进行分析;TSKgel® SuperSW mAb HR能在一次运行中为片段、单体和聚集体提供卓越的分离分辨率;TSKgel® UltraSW Aggregate涵盖更高的分子量,是分离抗体二聚体和更高的聚集体的最佳选择。请在以下网址获取最新的产品列表和订购信息sigma-aldrich.com/tsk。
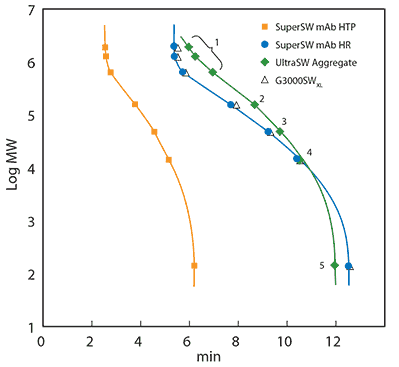
图 1.TSKgel® SuperSW mAb HTP(4.6 mm 内径 x 15 cm 长),TSKgel® SuperSW mAb HR,TSKgel® UltraSW Aggregate和TSKgel® G3000SWxl(均为7.8 mm内径x30 cm长)的校准曲线。
流动相:0.2 M磷酸钠缓冲液,pH 6.7,以及0.05%叠氮化钠。校准蛋白:甲状腺球蛋白(640 kDa),γ-球蛋白(155 kDa),白蛋白(47 kDa),核糖核酸酶 A(13.7 kDa)和ρ-氨基苯甲酸(0.14 kDa),均包含在15-600 kDa蛋白质标准混合物中 。上样量:10μL。流速:0.35 mL/min(4.6 mm内径)或1 mL/min(7.8 mm内径)。检测:UV @ 280nm
校准曲线显示了保留时间与一定范围内分子量之间的线性相关性。该分子量范围称为色谱柱的线性校准范围,可作为分离的最佳工作范围。如果样品不能在该洗脱范围内洗脱,则样品通常需要具有更小或更大孔的SEC柱。此外,适当的选择色谱柱和洗脱缓冲液可确保避免可能改变保留时间的二次互作。
蛋白质SEC的现成校准标准品
校准混合物应包含与分析样品分子相似的分子。尺寸排阻色谱法根据分子的流体动力学大小分离分子,这取决于水合壳的厚度。给定溶剂中的分子水合度由分子特征(如极性)决定。通常,聚乙二醇因其单分散性而用作标准品。用于校准的分子应该每个峰对应于一个分子量。此外,聚乙二醇非常稳定,可以在室温下储存多年。但不幸的是,对于蛋白质分析来说,聚乙二醇由于其更厚的水合壳而限制了其使用。对于使用SEC进行的蛋白质分子量测定来说,应采用蛋白质作为校准标准品。然而由于一些常出现的蛋白质相关的问题(例如蛋白质降解),使得校准标准品的处理变得更加复杂。因为该校准混合物是基于蛋白的,因此其具有有限的保质期,这意味着需要制备少量的标准品,以避免浪费大量的标准混合物。总之,准备工作可能需要耗费大量的时间。为避免制备标准品,请使用现成的标准品。
SEC蛋白质标准混合物可提供15 kDa至600 kDa的分子量范围。这使其能够进行大多数蛋白质的分子量测定。蛋白混合物装于2 mL管中,包含有冻干的蛋白粉和所有必需的缓冲离子。您只需加水并注入校准标准品。这使得您可以使用新制备的标准品进行快速简便的色谱柱校准。SEC应用于生物制药的QC分析,主要目的是定量样品组分,而不是确定分子量。对于这类的SEC分析,蛋白质标准溶液加样通常用于系统适用性测试。蛋白质标准品是帮助您制备系统适用性样品的便利工具。
色谱柱校准
在校准色谱柱时,使用与分析时相同的条件十分重要。更改缓冲体系会显著改变保留时间。例如,精氨酸是用于单克隆抗体(mAb)聚集分析的常用添加剂。它可以防止疏水性mAb聚集体和固定相[1,2和3]的二次相互作用,并缩短其在SEC中的保留时间(这也可能是由于水合壳略有改变)。图2 说明了加入200mM精氨酸对SEC中聚集的mAb样品液相的影响。
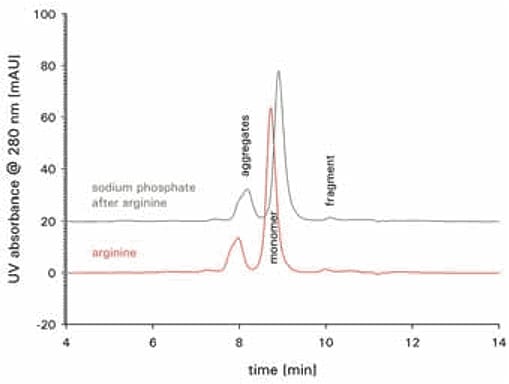
图 2.TSKgel® UltraSW Aggregate上的单克隆抗体样品,含0.1 M磷酸钠缓冲液,在流动相中含有0.2 M精氨酸(红色)。进样10次后,将流动相切换为含0.2 M硫酸钠(灰色)的磷酸钠缓冲液。对于两个流动相,均显示了第10次进样结果。色谱柱:TSKgel® UltraSW Aggregate。流速:1 mL/min。上样量:20μL。上样质量:100 µg。检测:UV @ 280nm。
如果参考在洗脱液中不使用精氨酸的情况下获得的校准标准品分离曲线,则所获得的保留位移(例如加入精氨酸后)将导致分子量计算错误。同样,从磷酸盐缓冲液转换到HEPES也观察到类似的效果(数据未显示)。除了所应用的液相之外,校准标准品的浓度和进样体积对于正确的保留时间和随后的分子量计算来说也是至关重要的。SEC色谱柱的重新装载会导致其分辨率降低,并可能导致保留时间的偏移。将典型的进样体积和标准品浓度进样至TSKgel® SuperSW mAb HR色谱柱上。将Sigma-Aldrich的蛋白质标准混合物溶于200μL、500μL和1000μL的水中。显然,高度浓缩的校准样品未得到很好的分离。在最大进样量(100μL)的结果中,该影响最为显著(图3)。
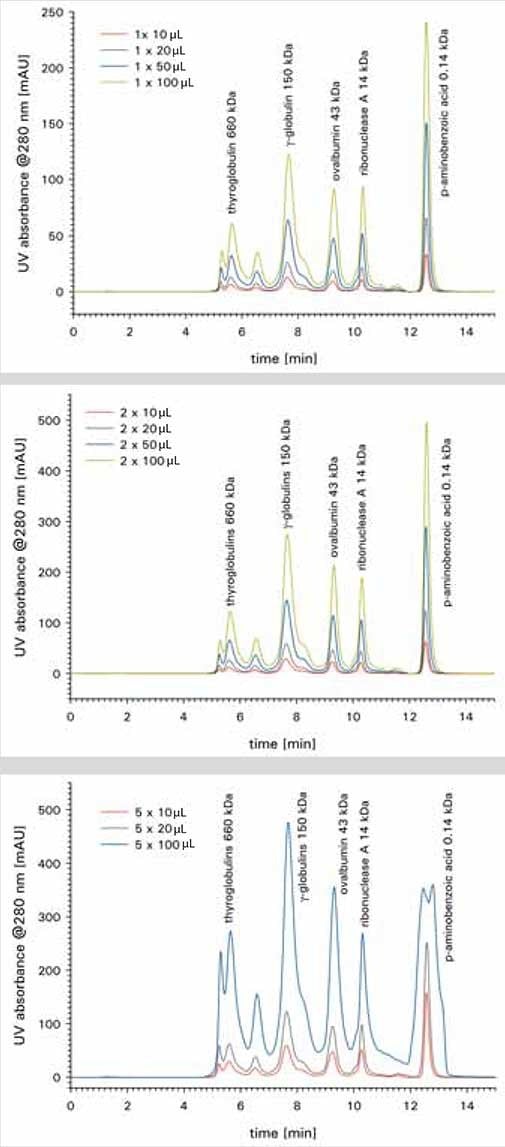
图 3.使用TSKgel® SuperSW mAb HR(7.8 mm 内径 x 30 cm 长)色谱柱分离蛋白质标准混合物15 - -600 kDa。进样量从5到100μL不等。该标准品以不同浓度进行制备:1X、2X 和 5X。洗脱缓冲液:200mM磷酸钠缓冲液,pH 6.7,以及200mM硫酸钠。流速:1 mL/min。检测:UV @ 280nm。
这些结果表明了适当的进样体积和浓度的重要性。只有这样才能计算出可靠的分子量。此外,色谱柱永久性过载可能导致色谱柱的提前老化。样品也是如此。研究人员需要将获得足够显著的信号所需的样品量与由于过载导致的色谱柱寿命缩短相平衡。通常,当注入1至5 mg/mL的20μL样品时,7.8 mm 内径 x 30 cm 长的色谱柱可获得最佳的分离结果和更长的使用寿命。
使用SEC进行分子量测定是一种具有良好准确性和再现性的分析方法。但是,需要考虑一些基本的方法参数。即用型校准标准品可以帮助您消除潜在的误差来源,例如进行低蛋白质量的称量。易于操作和适当浓缩的标准液可确保注入适当量的色谱柱校准或系统适应性测试。
参考文献
TSKgel是Tosoh Corporation的注册商标
如要继续阅读,请登录或创建帐户。
暂无帐户?