细胞培养实验方案10:通过Hoechst DNA染色检测细胞的支原体污染
目标

DNA染色(如间接Hoechst染色技术)一种快速的方法,其可在72小时内获得结果,这相较于通过培养分离检测支原体所需的4周时间相比是更加有利的。用DNA染色剂对细胞系进行直接染色可在24小时内获得结果,但会大大降低灵敏度(~106 cfu/mL)。这一问题可以通过将指示细胞系(如Vero)与试验细胞系共培养来改善。该富集步骤可获得100 cfu/mL培养物的灵敏度,并且是ECACC使用的优选方法。该步骤还可通过增加支原体可粘附的表面积来提高灵敏度。与通过培养进行检测一样,DNA染色法适用于从细胞培养物或细胞培养试剂中对支原体进行检测。
产品列表
- 细胞培养基 — 预热到适当的温度(有关正确的培养基和温度,请参阅ECACC细胞系数据表。)
- 甲醇(322415)
- 冰醋酸(A6283)
- Hoechst 33342染色液(B2261)
- 指示细胞如Vero细胞((84113001)
- 猪鼻支原体 NCTC10130和
- 口腔支原体 NCTC 10112
设备
- 个人防护装备(无菌手套、实验室外套、护目镜)
- 水浴温度设定为37 °C
- 具有防护等级的微生物安全柜
- CO2培养箱温度设定为37 °C
- 显微镜(紫外线外落射荧光)
- 组织培养皿
- 多培养皿12孔板
- 显微镜载玻片和13mm盖玻片
- 铝箔
操作流程
- 将无菌盖玻片置于组织培养皿/板(例如12孔板)中。
- 将2mL的指示细胞接种至准备好的培养皿中,例如12孔板每孔接种2×104 Vero细胞。
- 在37°C,5% CO2条件下孵育2-24小时,使细胞粘附在盖玻片上。
- 使用细胞刮刀将附着的测试细胞系置于悬浮液中。悬浮细胞系可进行直接检测。
- 从重复的培养皿中移除1mL培养物上清液,并向每个重复中加入1mL测试细胞样品。用100 cfu的每个阳性对照样品接种于2孔中。
- 将未接种的重复组织培养孔留作阴性对照。
- 将培养皿在37 °C,5% CO2中孵育3-5天。
- 3-5天后,通过向每个培养皿中加入至少2 mL新鲜制备的Carnoy's固定液(冰醋酸:无水甲醇=1:3)并保持3分钟,从而将细胞固定于盖玻片上。然后将固定液倒入有毒废物瓶中。重复一次该步骤。加入至少2mL Hoechst染色液(0.4μg/nl)。静置3分钟,避免光直射(如用铝箔覆盖)。
- 将使用和未使用的染色液倒入有毒废物瓶中。
- 将1滴封固剂加入预先标记的显微镜载玻片中,并将盖玻片(细胞侧朝下)置于载玻片上。
- 保持载玻片用铝箔覆盖,并将其放置在37 °C下至少15分钟或在室温下放置30分钟。
- 在100倍的紫外落射荧光下观察载玻片。
有效结果的标准
阴性对照显示无支原体感染;阳性对照显示支原体感染;Vero细胞可通过发荧光的细胞核清楚的观察到。
阳性结果的标准
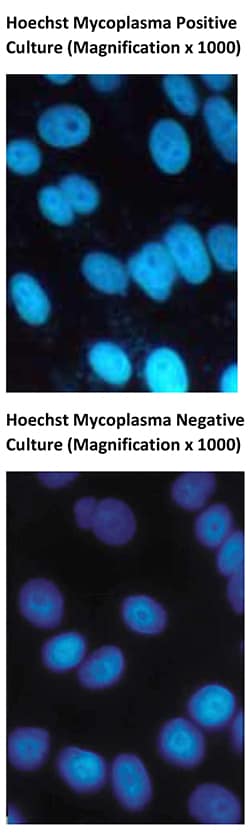
感染支原体的样品表现为:荧光细胞核,和支原体DNA(小球菌或细丝)的核外荧光。
阴性结果的标准
未感染的样品表现为:深色背景下发荧光的细胞核。应没有支原体的荧光证据,即支原体DNA的核外荧光。
注意
- DNA染色剂(如Hoechst染色剂)能与DNA特异性地结合。在所有培养物中,细胞核都会发生荧光。理论上,未污染的培养物仅显示出荧光核,而支原体阳性培养物则含有小的球菌或细胞,其可能吸附或未吸附于细胞上(图11)。但请注意,任何外来的DNA也可能产生荧光,例如细胞碎片 - 其有时会被误认为是支原体污染。
- Hoechst染色剂具有毒性,应小心处理和丢弃。
- 在某些情况下,结果可能难以解释,其原因可能为:
• 细菌/酵母/真菌污染
• 背景中碎片过多(如在如杂交瘤细胞系中)
• 因细胞全部死亡而导致的破裂细胞核
• 活细胞过少或没有 - 尽管该实验步骤建议使用阳性对照,但在资源有限的细胞培养设施中这可能是不可取的或不一定是可行的。如果要使用阳性对照,则应在与主要组织培养设施不同的实验室中进行。如果没有使用阳性对照,强烈建议您到独立的测试实验室定期测试您的细胞系。
- ECACC建议使用至少两种检测方法(例如间接DNA染色和培养物分离)对样品进行支原体检测,以获得更可靠的结果。这是由于不同种类的支原体对方法的检测灵敏度可能不同。
ECACC提供支原体检测服务,并可提供三种不同的检测方法:PCR、间接DNA染色和培养物分离。
登录以继续。
如要继续阅读,请登录或创建帐户。
暂无帐户?