酰胺键是有机化学中最重要的键之一,是肽、聚合物以及许多天然产物和药物中的关键官能团。 酰胺通常通过使用偶联试剂或事先将羧酸转化为衍生物来偶联羧酸和胺来制备。替代程序包括Staudinger连接,芳基卤化的氨基羰基化和醛的氧化酰胺化。然而,所有这些方法都需要化学计量量的各种试剂,并导致等摩尔量的副产物。在特殊情况下,酰胺可以通过催化程序形成,如酮和叠氮化物之间的施密特反应、贝克曼重排以及硫代酸与叠氮化物的酰胺化。
酰胺合成更环保的方案是胺与醇的直接酰胺化,其中释放出两个二氢分子。这种独特的转变在之前已经描述过,其中钌钳配合物用于空间位阻伯胺和醇的直接偶联。 1最近,Madsen等人报道了通过使用钌催化剂,N-杂环卡宾(NHC)和膦配体挤出二氢多根从醇和胺中合成酰胺(方案1)。阿拉伯数字
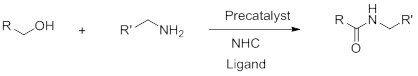
方案 1:催化酰胺键形成
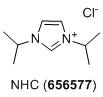
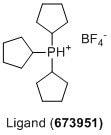
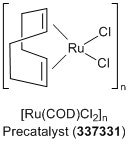
特殊危害: 腐蚀性物质、刺激物和易燃物(注意: 要全面了解所有相关危害,请参阅 MatNo 每个组件的 SDS)。
一般实验程序:
- 将 500 mL 4 颈反应瓶组装在带有冷凝器的加热罩中,顶部有一个大口径旋塞阀,通向氩气起泡器和温度计。
- 用氩气冲洗烧瓶30分钟。
- 给 [Ru(COD)Cl2]n、PCyp3 充电。HBF4,1,3-二异丙基氯化咪唑和吨BuOK在 氩气压力下使用粉末漏斗放入反应瓶中。
- 通过抽真空和回填氩气对固体进行脱气,总共三个循环;之后,将反应瓶置于轻微的氩气正压下。
- 在氩气压力下使用套管给甲苯充电。
- 将反应混合物回流30分钟。观察到深色或黑色溶液。
- 将反应混合物冷却至室温。
- 在氩气压力下加入酒精和胺。
- 将反应混合物在加热套中的氩气气氛下回流24小时。
- 将反应混合物冷却至室温,并在真空中 除去溶剂 。
- 将残留物吸附到硅胶上,并通过柱层析(淋洗液:己烷/EtOAc 8:2至7:3)纯化以得到酰胺。
代表性示例:
第一次实验用2-苯乙醇和己胺进行,以验证文献方法(方案2)。
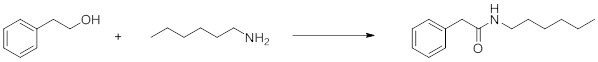
方案2:2-苯乙醇与己胺的酰胺化
N-己基-2-苯基乙酰胺: [Ru(COD)Cl2]n, PCyp3·将HBF4,1,3-二异丙基咪唑氯化物和 tBuOK置于干燥的舒伦克管中。施加真空,然后将管中充满氩气(重复两次)。加入甲苯,将混合物在氩气气氛下在油浴中加热回流20分钟。将烧瓶从油浴中取出,并加入酒精和胺。将混合物在油浴中的氩气气氛下回流加热24小时。将反应混合物冷却至室温并在真空中除去 溶剂。残余物通过硅胶柱色谱法(洗脱液:己烷/EtOAc 8:2至7:3)纯化以得到酰胺。
在掌握优化条件后,我们将该方法应用于含有氮杂环(方程1)和受保护胺(等式2)的脂肪醇(方案3),以研究该方法的范围和局限性。

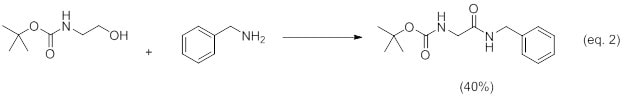
方案3:胺和醇的酰胺化。
引用
如要继续阅读,请登录或创建帐户。
暂无帐户?