肽合成_多肽_固相肽合成-默克生命科学
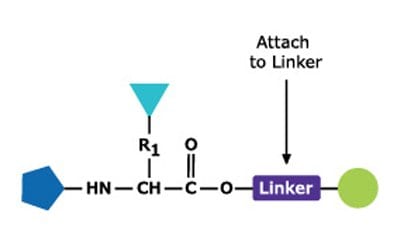
肽由两个或多个氨基酸通过酰胺键连接而成,形成一条氨基酸链,长度一般为 2 - 70 个氨基酸。肽与蛋白质的区别在于,肽不需要折叠就能发挥生物活性。肽作为肽类激素(如血管紧张素、LHRH、脑啡肽)以及毒素存在于动植物体内。肽作为药物发现的先导化合物和药物本身都具有极大的研究价值。肽还可用于疫苗、生物材料、组织学探针,并被大量用作抗原以产生抗体。
肽是在溶液或固相中通过化学方法合成的。合成过程包括在一个受 N 保护的氨基酸与一个带有游离氨基和受保护羧酸的氨基酸之间定向和选择性地形成酰胺键。在固相合成中,羧基保护基团与聚合物支架相连。键形成后,二肽的氨基保护基团被移除,然后连接下一个 N 保护氨基酸。
特色类别
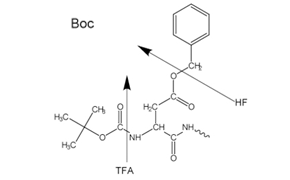
Figure 2Side-chain protecting groups for Boc solid-phase peptide synthesis (SPPS)
固相肽合成(SSPS)因其高效、简单、快速和易于并行化而成为最常用的肽合成方法。SPPS 是指将氨基酸残基和侧链保护氨基酸残基依次加到附着在 可溶性聚合物支持(图 1)。
无论是酸亲和性叔丁氧羰基(Boc SPPS)还是碱亲和性Fmoc-group(Fmoc SPPS)用于 N-α 保护。去除该保护基团后,使用偶联试剂或预活化的保护氨基酸衍生物加入下一个保护氨基酸。C 端氨基酸通过链接器锚定到树脂上。>链接剂,其性质决定了肽链延伸后从支持物中释放所需的条件。通常选择侧链保护基团,以便在肽与树脂分离的同时被裂解(图 2和3)。
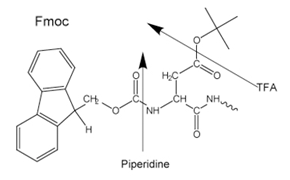
Figure 3.Side-chain protecting groups for Fmoc solid-phase peptide synthesis (SPPS)
相关文章
- Novabiochem® offers a wide range of linkers and derivatized resins for Fmoc solid-phase peptide synthesis with specialized protocols.
- Chromogenic and fluorogenic derivatives are invaluable tools for biochemistry, having numerous applications in enzymology, protein chemistry, immunology and histochemistry.
- Aspartimide formation 1,2 is caused by repeated exposure of aspartic acid-containing sequences to bases like piperidine and can result ultimately in the generation of 9 different by-products.
- Novabiochem® offers polymer supports for solid phase peptide synthesis, suitable for various peptide lengths and sequences.
- Long peptide purification removes impurities effectively, crucial for research and pharmaceutical applications.
- 查看全部 (13)
相关协议
- A guide to create solvent systems used for the thin-layer chromatography assay of Novabiochem products.
- Overcome challenges in synthesis and disulfide bond formation with protocols for Fmoc solid-phase peptide synthesis of peptides with cysteine and methionine.
- We provide an overview of our available reagents, together with recommendations and details of their use for synthesis of peptides containing post-translationally modified amino acids.
- Anhydrous HF is the preferred reagent for peptide cleavage from Boc-based resins, versatile and effective for various peptide synthesis.
- Fmoc resin cleavage and deprotection are crucial steps for peptide synthesis, yielding the desired peptide after resin detachment.
- 查看全部 (7)
查找更多文章和协议
我们能提供哪些帮助
如有任何问题,请提交客户支持请求
或与我们的客户服务团队联系:
发送电子邮件custserv@sial.com
或致电 +1 (800) 244-1173
额外支持
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- 计算器与应用_缓冲液计算器_HPLC方法转换计算器-默克生命科学
默克该工具箱包括用于化学、生命科学、材料科学等方面的科学研究工具和资源。
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
如要继续阅读,请登录或创建帐户。
暂无帐户?